«Железное» решение
В Северо-западном университете (шт. Иллинойс) и Аргоннской национальной лаборатории (ANL, шт. Чикаго) создан аккумулятор с уникальной электрохимией. «Наши численные модели показали, что аккумулятор весьма перспективен, - рассказал Кристофер Вольвертон, профессор материаловедения Школы инженерных наук им. МакКормика при Северо-западном университете. - Замечательно, что он реально работает».
Ионно-литиевые аккумуляторы, если без лишних подробностей, работают благодаря тому, что ионы лития перемещаются из анода в катод и наоборот. При зарядке ионы направляются на «хранение» в катод, который изготавливается из материала, содержащего литий, кислород и переходный металл. В большинстве случаев переходный металл - это кобальт.
«В обычных аккумуляторах реакция происходит именно с переходным металлом, - рассказывает К. Вольвертон. - И поскольку на один атом кобальта приходится лишь один ион лития, объём сохраняемого заряда оказывается небольшим. Хуже того, продуктивно используется лишь половина лития, имеющегося в катоде».
Между тем в таблице Менделеева присутствуют и иные переходные металлы, например, недорогое железо. Именно его применила группа Вольвертона вместо кобальта, заодно вовлекая в реакцию кислород.
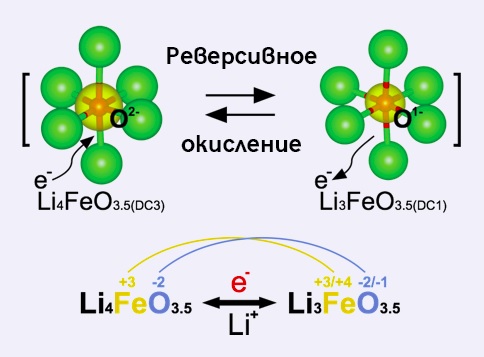
Кислород тоже способен присоединять и высвобождать ионы лития, что позволяет нарастить ёмкость аккумуляторов без увеличения их массы. Многие исследователи пытались это сделать, но мало кто смог получить работающие образцы аккумуляторов. Когда кислород начинал участвовать в реакции, химические соединения теряли стабильность. Кроме того, кислород выделялся в виде газа и выходил из аккумулятора, отчего реакция становилась необратимой.
С помощью машинного моделирования группа исследователей рассчитала оптимальное соотношение компонентов - такое, чтобы кислород не выделялся, а также связывался. И теперь на один атом переходного металла (железа) приходятся четыре иона лития. Аккумулятор получается недорогим, а его удельная ёмкость увеличивается вчетверо.





















